Maladie de Crohn

Mise à jour
05/11/2021
INTRODUCTION/GÉNÉRALITÉ
Votre texte ici
HISTORIQUE
Votre texte ici
PHYSIOPATHOLOGIE
Votre texte ici
ÉPIDÉMIOLOGIE
Votre texte ici
FACTEURS DE RISQUES
Votre texte ici
EXAMEN CLINIQUE
Votre texte ici
EXAMENS COMPLÉMENTAIRES
Votre texte ici
DIAGNOSTICS DIFFÉRENTIELS
Votre texte ici
ÉTIOLOGIE
Votre texte ici
COMPLICATIONS
Votre texte ici
PRISE EN CHARGE THÉRAPEUTIQUE
A) Chirurgie dans la maladie de Crohn 1
1) Recommandations générales
- La laparoscopie est la voie d’abord chirurgicale de référence. Elle réduit la morbidité globale, la durée d’hospitalisation, les adhérences post-opératoires, le risque d’éventration et apporte un bénéfice esthétique.
- Une prise en charge des stomies par une stomathérapeute spécialisée permet d’améliorer la qualité de vie des patients et de réduire les coûts.
- Les risques de syndrome du grêle court sont : interventions chirurgicales répétées, complications chirurgicales nécessitant une réintervention et phénotype agressif de la MC (EL4).
- Une optimisation péri-opératoire des patients menée en accord avec les principes ERAS (Enhanced Recovery After Surgery) est recommandée. Elle comprend l’arrêt du tabac et de l’alcool, l’absence de préparation colique, un jeûne pré-opératoire limité à 2 heures pour les liquides et 6 heures pour les solides, une limitation dans l’utilisation des morphiniques, une réalimentation et une mobilisation précoces après la chirurgie.1 1 Cette prise en charge optimale permet de réduire la durée d’hospitalisation et le taux de complication post-opératoire.1
2) Indications opératoires
a) En urgence
- Les indications de chirurgie en urgence représentent environ 6 à 16 % des cas.1 Elles sont dominées par la péritonite par perforation en péritoine libre et l’hémorragie massive ne répondant pas au traitement médical.
- En cas de colite aiguë de MC résistante au traitement médical optimal après une semaine ou présentant des signes de gravité (détérioration clinique), une chirurgie en urgence doit être discutée. Les modalités du traitement sont similaires à ceux de la colite aiguë en cas de RCH avec une colectomie sub-totale et double stomie.1
- En cas d’occlusion aiguë par une sténose ou une inflammation digestive, le traitement médical doit être proposé en première intention. Pour les formes inflammatoires actives, les stéroïdes sont utilisés en première intention.1 La chirurgie en urgence est indiquée avec résection du segment malade si une ischémie digestive est suspectée. En cas d’occlusion ne répondant pas au traitement médical, après optimisation du patient (nutrition, statut immunitaire…), la chirurgie est habituellement programmée. De même en cas d’abcès intra-abdominal, la chirurgie en urgence n’est indiquée qu’en cas d’absence de réponse au traitement médical et si aucun drainage percutané n’est possible.
b) En électif
- En cas de MC iléo-caecale avec symptômes obstructifs sans signe d’inflammation active, la chirurgie est la meilleure option thérapeutique.
- Les patients avec une atteinte inflammatoire doivent être traités préférentiellement médicalement. La chirurgie est indiquée en cas d’échec thérapeutique.
- Les MC perforantes symptomatiques doivent être considérées pour la chirurgie à un stade précoce. Il existe en effet un risque élevé de non-réponse au traitement médical.
- En cas d’abcès traité médicalement avec succès, plusieurs études préconisent la résection à distance de l’épisode.1
- En cas de MC pédiatrique, la chirurgie doit être considérée à la puberté ou en pré-puberté en cas de cassure de la courbe de croissance après 6-12 mois de traitement médical optimal et de support nutritionnel.
3) Prise en charge péri-opératoire
- Les stéroïdes doivent être arrêtés avant la chirurgie si possible car ils augmentent la morbidité chirurgicale (équivalent Prednisone 20 mg pendant plus de 6 semaines). En cas de prise de stéroïdes au long cours, une substitution est indispensable en post-opératoire afin d’éviter l’insuffisance surrénale aiguë.
- Les anti-TNF augmentent le taux de complications septiques intra-abdominales post-opératoires après résection pour MC. Le délai d’arrêt des Anti-TNF avant une chirurgie est inconnu. Habituellement un délai de 6-8 semaines après la dernière injection est considéré comme suffisant.1 Les thiopurines peuvent être poursuivies en péri-opératoire et en post-opératoire.
- La mise en condition des patients présentant un abcès intra-abdominal comprend un traitement antibiotique plus ou moins associé à un drainage percutané avant une résection chirurgicale. On considère habituellement qu’un abcès de plus de 5 cm de diamètre nécessitera un drainage. Dans tous les cas, avant chirurgie pour MC, un bilan des localisations de la MC et une exploration récente du tractus digestif bas (iléo-coloscopie et imagerie) sont nécessaires. Les recommandations ECCO-ESGAR stipulent que l’entéro-IRM est l’examen de choix pour la MC.1
- La dénutrition est un facteur majeur de morbidité postopératoire.1 Le statut nutritionnel doit être optimisé avant la chirurgie par voie entérale ou parentérale. En cas de chirurgie chez un patient dénutri, une résection sans anastomose doit être évoquée. L’albumine n’est pas toujours un bon reflet de l’état nutritionnel des patients car elle est modifiée par l’inflammation et/ou le sepsis.
- Les patients avec une MC opérés sont à haut risque de thrombose veineuse profonde et une prophylaxie est indiquée sauf contre-indication. La prophylaxie doit durer 28 jours. Pour les MC pédiatriques, le risque de thrombose est plus faible et la prophylaxie doit être discutée au cas par cas.
4) Spécificités par localisation anatomique
a) Tractus digestif supérieur
- Les atteintes du tractus digestif supérieur sont plus fréquentes chez les enfants, mais la chirurgie n’est pas plus fréquemment nécessaire. Ce sont surtout les sténoses symptomatiques qui vont nécessiter un traitement chirurgical. Les sténoses sont localisées préférentiellement dans l’antre et le bulbe duodénal (50-60 %) puis le D2-D3 (25-30 %) et plus rarement dans le duodénum distal (10-15 %). 10 % des patients auront des sténoses multiples.
- Œsophage : Les atteintes sont rares et sont quasiment toujours associées à des manifestations extra-digestives.1 La place de la chirurgie est très limitée. Les lésions nécessitent principalement des dilatations endoscopiques.
- Estomac : en cas d’indication chirurgicale, il s’agit le plus souvent d’une dérivation par anastomose gastro-jéjunale ou d’une gastrectomie distale. La vagotomie de principe est contre-indiquée.
- Antre-Duodénum (D1) : Les deux procédures de choix sont la stricturoplastie et la dérivation avec une anse en Y.
- Duodénum (D2-D3) : Les sténoses peuvent être traitées efficacement par stricturoplastie. La duodénectomie ou la pancréatico-duodénectomie ne doivent être évoquées qu’en dernier ressort. La vagotomie de principe est contre-indiquée.
- En cas de fistule interne impliquant l’estomac ou le duodénum, un geste conservateur est à préférer (suture directe, résection latérale, stricturoplastie).
b) Jéjunum-iléon
- Les facteurs de risque de résection et de récidives chirurgicales sont un début de la maladie au cours de l’enfance, la localisation jéjuno-iléale et le phénotype perforant. Au cours d’une intervention chirurgicale, après le bilan exhaustif des lésions (nombre, localisation, type), le traitement doit être adapté à chaque segment selon leurs caractéristiques.
- Une forme sténosante courte opérée pour la première fois peut être traitée par une résection courte ou une stricturoplastie.
- Une forme sténosante multiple doit être préférentiellement traitée par des stricturoplasties multiples si elles sont possibles.
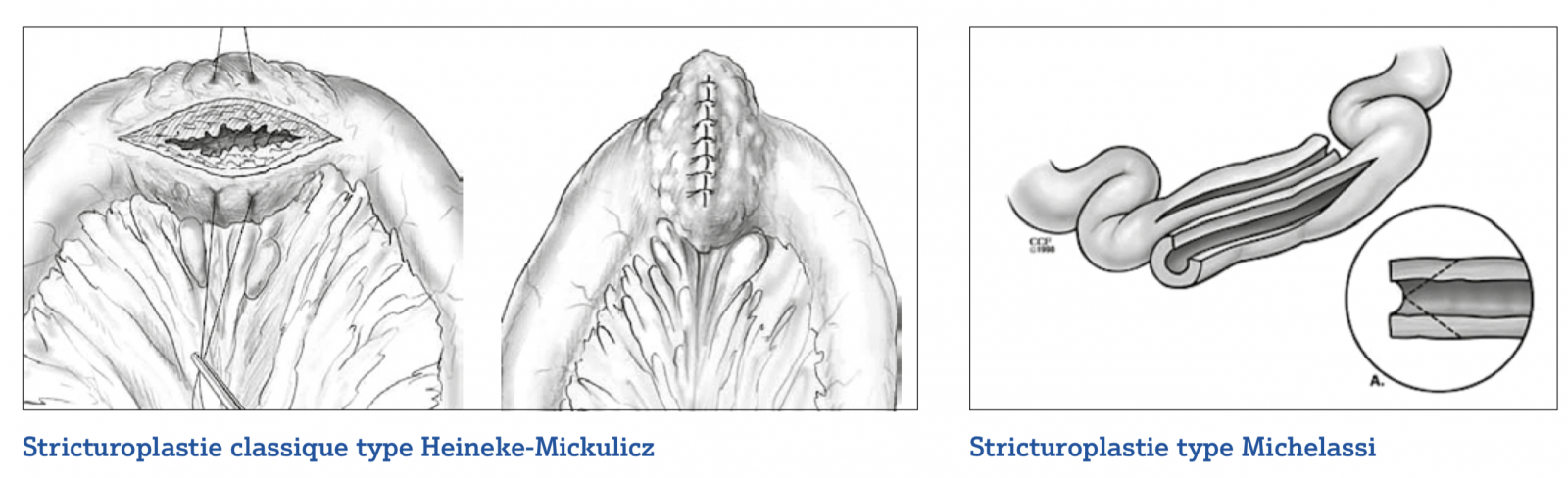
- La taille de la sténose doit être inférieure à 10 cm pour pouvoir réaliser une stricturoplastie classique type Heineke-Mickulicz.
- Les sténoses longues (> 20 cm) exposant à un risque de sacrifice digestif important doivent être traitées par des stricturoplasties type Michelassi.
- La stricturoplastie type Finney n’est pas réalisée en pratique, car elle expose à une pullulation bactérienne en raison du diverticule géant qui est créé.
- Le risque de cancer sur une stricturoplastie est très faible (0,5 %) et les biopsies systématiques de la muqueuse en cas de stricturoplastie ne sont pas recommandées.1
c) Iléon terminal
- La voie d’abord laparoscopique est recommandée pour les résections iléo-caecales. Dans les centres experts, la laparoscopie peut également être proposée pour les formes complexes ou les récidives. Le risque de conversion est plus élevé mais la morbidité semble équivalente.
- En cas de forme perforante, la résection iléo-caecale est fortement recommandée. En cas de forme sténosante, le choix entre la résection et la stricturoplastie iléo-colique est possible, ces deux techniques donnant les mêmes résultats en termes d’efficacité et de récidive. La dilatation endoscopique est considérée comme la procédure de choix pour les sténoses courtes. Elle doit être réalisée dans les centres disposants d’une unité chirurgicale. La sténose doit être inférieure à 4 cm. Une dilatation itérative est nécessaire dans 20 % et 50 % des cas à 1 et 5 ans, respectivement. L’anastomose doit être la plus large possible et les sutures latéro-latérales sont donc recommandées.
- L’appendicectomie d’un appendice macroscopiquement sain en présence d’un iléon terminal inflammatoire est associée à un risque élevé de complication septique intra-abdominale et de fistule.1
- Les facteurs de récidive après résection iléo-caecale sont : tabac, antécédent de résection chirurgicale, absence de traitement prophylactique, phénotype perforant, association à des lésions ano-périnéales, présence de granulome ou de plexite sur le spécimen. Il est maintenant prouvé qu’un traitement par Anti- TNF réduit le risque de réintervention. Tous les patients présentant au moins un facteur de risque doivent recevoir un traitement adjuvant à la chirurgie. Une iléo-coloscopie est recommandée dans l’année suivant la résection pour détecter une récidive précoce endoscopique (à classer selon Rutgeerts 21) et modifier le traitement prophylactique.
d) Côlon
- Le traitement de choix des sténoses coliques est la dilatation endoscopique ou la résection segmentaire. Le risque de réintervention après résection segmentaire est d’environ 30 %. Les facteurs de risque de résection itérative sont : le sexe féminin, des LAP et un début précoce de diagnostic de la maladie.1 Les stricturoplasties ne sont pas recommandées en cas de sténose colique principalement en raison du risque de cancer 1 et par manque de données.
- En cas de sténose touchant deux segments coliques, une double résection peut être envisagée. Cependant, la colectomie totale permet de réduire le risque de complication post-opératoire et apporte un bon résultat fonctionnel (> 70 % à 10 ans).1
- En cas de pancolite réfractaire au traitement médical, une iléostomie de dérivation peut être proposée. Après la rémission, une colectomie totale avec anastomose iléo-rectale ou une intensification du traitement médical peuvent être proposées (EL5).
- Chez des patients sélectionnés sans antécédent de lésion ano-périnéale et d’atteinte de l’intestin grêle, une coloproctectomie totale avec anastomose iléo-anale peut être proposée et offre la même qualité de vie qu’en cas de recto-colite hémorragique même si le taux de perte du réservoir à long terme est augmenté. Les patients ayant une anastomose iléo-anale chez qui on découvre a posteriori une MC ont une morbidité et un risque de perte du réservoir augmentés. Une prise en charge multidisciplinaire est indispensable pour garder le plus longtemps possible la fonction du réservoir. La réfection d’un réservoir iléal en cas de MC n’est pas habituellement recommandée au vu des risques post-opératoires, notamment le taux de sepsis pelvien chronique très important.1
- Pour les MC pédiatriques, en cas de retard de croissance, l’iléostomie de dérivation n’a pas la même efficacité que la résection du segment malade. Cela a été prouvé pour l’ensemble des résections pour les MC.1 La résection colique précoce en cas de MC réfractaire au traitement médical permet de récupérer la croissance. Le timing de la colectomie chez l’enfant dépend de multiples facteurs : croissance, parcours scolaire, traitement médical, phénotype de la MC.
e) Lésions ano-périnéales (LAP)
- Dans les études de population, l’incidence des LAP varie entre 14 et 23 % avec une incidence cumulée dépendant du délai depuis le diagnostic.1 Le risque de développer une atteinte anale avec fistule dépend également de la localisation de la maladie digestive. En cas de maladie colique avec atteinte rectale, l’incidence monte à 92 % 30.
- Le bilan initial d’une LAP doit comporter une IRM pelvienne et une endoscopie recto-sigmoïdienne à la recherche d’une inflammation. La fistulographie n’est pas recommandée.
- En cas de fistule symptomatique, la mise en place d’un séton associée à une antibiothérapie est le traitement de choix. En cas de fistule simple récidivante, les thiopurines ou les Anti-TNF sont la deuxième ligne de traitement à proposer.
- Les traitements d’entretien des LAP sont : les thiopurines, les Anti-TNF, les autres biotherapies et la pose d’un séton. Pour les patients réfractaires au traitement médical, la confection d’une stomie doit être évoquée. La proctectomie ne doit être discutée qu’en dernier recours.
- La chirurgie de fermeture d’une fistule anale en cas de MC peut être proposée en cas de : patient asymptomatique, sans abcès concomitant, avec une rectite contrôlée médicalement et sur un trajet fistuleux bien défini anatomiquement. Le type de procédure chirurgical dépend des caractéristiques du trajet fistuleux, de l’anus (sténose, état, anciennes procédures réalisées) et de l’expertise du chirurgien. Plusieurs techniques sont disponibles (fistulotomie simple, séton au long cours, flap d’avancement muqueux, LIFT (ligature inter-sphinctérienne du trajet), colle biologique, plug… La fistulotomie est recommandée pour les fistules sous-cutanées ou superficielles. Elle est cependant contre-indiquée en cas de MC très active (CDAI > 150) ou de maladie périanale importante et il n’est recommandé de réaliser des fistulotomies antérieures chez la femme. Ces dernières exposent à un risque important d’incontinence anale.
- Les sétons (sans traction) permettent de drainer la fistule, réduire le risque de nouvel abcès ou de transformation en fistule complexe. En cas de rectite modérée ou sévère la pose d’un séton est la seule technique possible. La simple pose d’un séton en association avec le traitement médical peut guérir une fistule. La probabilité de fermeture de la fistule après le retrait varie entre 14 % et 100 %. Elle est plus probable en l’absence d’abcès, de rectite ou de sténose. Le séton doit donc être retiré après la phase d’induction de l’anti-TNF (en moyenne 4 semaines) et la disparition de la rectite. Il n’est pas recommandé d’utiliser des sétons avec traction progressive en cas de LAP de CD car il existe un risque de déformation anale et d’incontinence fécale (57 %).1
- Une stomie de dérivation est efficace sur les symptômes de LAP de MC dans 2/3 des cas et peut améliorer la qualité de vie des patients. Seuls 20 % des patients auront une fermeture de cette stomie au long cours. Les facteurs de risque de stomie définitive sont la sténose rectale et la colite de Crohn associée. Selon les séries anciennes, le taux de proctectomie varie entre 8 % et 40 %. Pour les patients ayant des facteurs de risque de stomie définitive, la chirurgie de résection doit être envisagée plus rapidement. Depuis l’avènement des traitements biologiques, le taux de stomie permanente a diminué de 60 % à 19 %.1
f) Cancers digestifs et MC
- En cas de cancers ou de dysplasie de haut grade sur une colite de MC, une coloproctectomie totale doit être considérée chez les patients pouvant supporter une intervention en raison du caractère multifocal de la dysplasie et du risque élevé de cancer métachrone en cas de résection segmentaire. En cas de dysplasie de bas grade ou de patients à haut risque chirurgical, une surveillance endoscopique intensive ou une colectomie segmentaire peuvent être discutées.
- En cas de cancer de l’intestin grêle le traitement recommandé est : une résection large emportant le mésentère pour les cancers du grêle, une colectomie droite carcinologique pour les cancers de l’iléon terminal et la duodénopancréactectomie céphalique pour les cancers du duodénum.
- La dégénérescence tumorale de LAP de MC est rare. La clinique, l’imagerie et l’endoscopie ont une faible sensibilité. Un examen sous anesthésie générale avec des biopsies des zones suspectes est indispensable. Le traitement chirurgical doit suivre les recommandations de chirurgie oncologiques.1
ÉVOLUTION/PRONOSTIC
Votre texte ici
PRÉVENTION
Votre texte ici
SURVEILLANCE
Votre texte ici
CAS PARTICULIERS
Votre texte ici
THÉRAPIES FUTURES
Votre texte ici
